Signalwege der Anpassung an das Ausdauertraining
Jeder weiss, dass regelmässiges Ausdauertraining zur Verbesserung der Ausdauerfähigkeit führt. Doch welche Anpassung an das Ausdauertraining können im Körper erwartet werden. Wir klären dich auf in diesem Blog.
Regelmässige, trainingsinduzierte Reize verbessern jeweils verschiedene Komponenten der Ausdauerfähigkeit. Diese Anpassungen an das Ausdauertraining finden einerseits zentral (Verbesserung des Herzminutenvolumens) und andererseits peripher in der Arbeitsmuskulatur (Muskelfaserverteilung, Mitochondriendichte, Kapillarisierung) statt. Dabei ist vor allem zu beachten, dass die zentralen Adaptationen unabhängig vom gewählten Trainingsmittel verbessert werden, die peripheren Anpassungen dagegen vorwiegend in der eingesetzten Muskulatur stattfinden. Aufgrund dessen sollte die Wahl des Trainingsmittels gut überlegt und vor allem dem individuellen Ziel angepasst sein.
Wie es durch die verschiedenen Arten des Ausdauertrainings zu spezifischen Anpassungen kommt und wie diese zum Teil, durch eine geeignete Wahl der Trainingsmethode, bewusst gesteuert werden können ist Teil der sportphysiologischen Forschung und wird hier in einem kurzen Überblick, für das grobe Verständnis zusammengefasst.
1. Anpassung an das Ausdauertraining: Athletenherz oder pathologische kardiale Hypertrophie.
Die Hauptkomponente der zentralen Anpassung durch Ausdauertraining ist eine vorwiegend strukturelle Veränderung des Herzmuskels. Diese Veränderungen können einerseits positiv (Athletenherz) und andererseits auch negativ (hypertrophe Kardiomyopathie) ausfallen. Beim Athletenherz vergrössert sich vorwiegend der linke Ventrikel und die Herzmuskelwand verdickt sich dazu im richtigen Verhältnis, was Netto zu einem vergrösserten Schlagvolumen führt (das Herz kann pro Schlag mehr Blutvolumen auswerfen). Beim Herzkranken Patienten dagegen (z.B. durch eine Aortenstenose oder eine langjährige Hypertonie) nimmt die Wanddicke auf Kosten des Ventrikelvolumens stark zu, was schlussendlich zu einem verringerten Schlagvolumen führt und nach einer meist langjährigen Herzinsuffizienz, durch Versagen des Herzmuskels, im Herztod endet.
Wie zu erwarten führen zwei verschiedene molekulare Signalwege zu den erwähnten Anpassungen am Herzmuskel. Vor allem wiederholte Intervalle von intensiven Ausdauerbelastungen führen durch Erhöhung der Konzentrationen von PI3K und anschliessend PKB/Akt und Erniedrigung des C/EBPbeta Signalweges zu einer physiologischen Hypertrophie der Herzmuskelzellen. Die pathologische kardiale Hypertrophie dagegen beruht vorwiegend auf einem gesteigertem Calcineurin Signal.
Vielleicht wird es früher oder später möglich sein, auf diese Signalwege mittels Medikamenten oder genetischen Methoden einen direkten Einfluss auszuüben.
Sicher ist jedoch die Möglichkeit der Einflussnahme durch wiederholtes intensives Ausdauertraining oder das Beheben von den begünstigenden Faktoren für eine hypertrophe Kardiomyopathie (Blutdruckregulation, Aortenstenosenoperation usw.)
2. Anpassung an das Ausdauertraining: Anpassungen in der Muskelfaserverteilung.
Eine wichtige strukturelle Komponente auf muskulärer Ebene für die Ausdauerleistungsfähigkeit ist die Muskelfaserverteilung. Grundsätzlich lassen sich die menschlichen Skelettmuskelfasern in langsam kontrahierende Typ 1 und schnellkontrahierende Typ 2a (schnell) und Typ 2x (sehr schnell) Fasern einteilen. Die Namen dieser Einteilung basieren auf den schweren Myosinketten, welche vor allem in Skelettmuskelfasern exprimiert werden. Typ 2x Fasern exprimieren zum Beispiel vorwiegend schwere Myosinketten vom 2x Typ.
Es konnte diesbezüglich gezeigt werden, dass in Typ 1 Muskelfasern vorwiegend der Calcineurin-NFAT Signalweg induziert wird. Wird dieses Signal durch einen spezifischen Inhibitor abgeschwächt, verkleinert sich das Verhältnis der Typ1 zu den Typ2 Fasern. Dieses Signal wird ausserdem durch langanhaltende elektrische Stimulation in Modellorganismen gesteigert, was einen Zusammenhang der Muskelfaserverteilung mit körperlichem Training indiziert. Zu den Typ 2 Fasern konnte einen durch Ausdauertraining induzierten Wechsel von Typ 2x auf Typ 2a Fasern gefunden werden, was eine leichte Verlangsamung auf Faserebene vermuten lässt. Insgesamt wird der Muskel durch trainingsinduzierte Reize natürlich nicht langsamer. Einen Wechsel von Typ1 auf Typ2 Fasern und umgekehrt kann theoretisch durch jahrelanges Training begünstigt werden, die Evidenz dafür ist jedoch sehr limitiert, was keine definitive Aussage ermöglicht.
Was dagegen mit Sicherheit gezeigt werden konnte, ist das gegenseitige Unterdrücken der Genexpression der einzelnen schweren Myosinkettentypen untereinander. Dies erklärt die Tatsache, dass in einem gewissen Muskelfasertyp jeweils nur ein Typ der schweren Myosinketten exprimiert und alle anderen unterdrückt werden.
3. Anpassung an das Ausdauertraining: Trainingsinduzierte mitochondriale Biogenese.
Regelmässiges Ausdauertraining führt mit der Zeit zu einer Erhöhung der Dichte an Mitochondrien im Muskel. Diese Anpassung an das Ausdauertraining wird mitochondriale Biogenese genannt und kann grundsätzlich mit zwei Signalwegen erklärt werden. Langanhaltendes langsames Ausdauertraining führt durch die Freisetzung von Kalzium zu einer Aktivierung von CaMK. Während eines hochintensiven Intervalltrainings (HIIT) werden dagegen von AMPK die tiefen Konzentrationen von AMP und ADP registriert. Diese registriert ausserdem den Abfall des Glykogens.
AMPK und CaMK steigern die Expression des Transkriptionsfaktors PGC-1alpha, welcher seinerseits mittels Expressionssteigerung der nukleären und mitochondrialen DNA die mitochondriale Biogenese verbessert.
4. Anpassung an das Ausdauertraining: Trainingsinduzierte Angiogenese.
Ein leistungslimitierender Faktor in Ausdauersportarten ist wie bereits beschrieben neben der maximalen Sauerstoffaufnahme auch die periphere Sauerstoffverwertung. Diesbezüglich ist vor allem die Dichte des muskulären Kapillarnetzes von zentraler Bedeutung.
Über den CaMK/AMPK-PGC-1alpha Signalweg, hypoxieinduziertes-HIF-1 und scherstressinduziertes-NO werden angiogene Wachsumsfaktoren (fördern das Kapillarwachstum) heraufreguliert. Einer der wichtigsten dieser Faktoren ist VEGF (vascular endothelial growth factor).
Ausserdem wird durch Ausdauertraining die Expression von Metalloproteinasen gesteigert, welche die extrazelluläre Matrix für ein Aussprossen der Kapillaren, durch das Bilden von Tunnels vorbereiten.
Zusammenfassung
Wie oben beschrieben können grundsätzlich 4 Anpassungen an das Ausdauertraining erwartet werden:
- Anpassung des Herzens: Vergrösserung der linke Herzkammer und der Herzmuskelwand. Dies führt zu einem vergrösserten Schlagvolumen.
- Anpassungen in der Muskelfaserverteilung: Die Muskelfasern werden ausdauernder (Veränderung von Typ IIx zu Typ IIa)
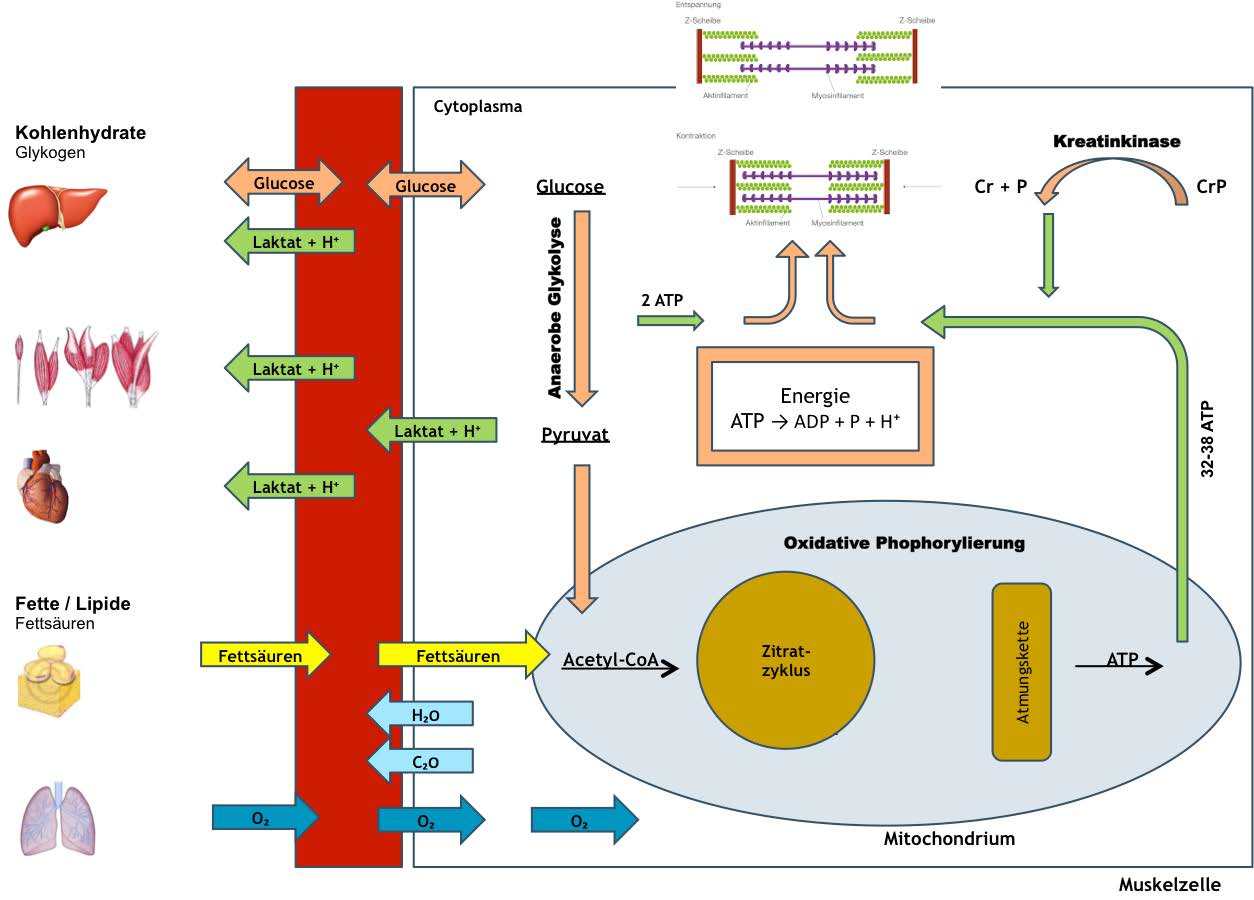
- Mitochondriale Biogenese: Erhöhung der Dichte an Mitochondrien im Muskel. Die Mitochondrien sind die Kraftwerke der Zellen.
- Angiogenese: Erhöhung der Dichte des muskulären Kapillarnetzes. Die Kapillaren sind feinste Verzweigungen der Blutgefässe).

Quellen
- Wackerhage H. Molecular Exercise Physiology. Abingdon: Routledge; 2014. 24-30, 52-65, 79-111, 133-151 p.
- Scharhag J, Schneider G, Urhausen A, Rochette V, Kramann B, Kindermann W. Athlete’s heart: Right and left ventricular mass and function in male endurance athletes and untrained individuals determined by magnetic resonance imaging. J Am Coll Cardiol. 2002;40(10):1856–63.
- Bernardo BC, Weeks KL, Pretorius L, McMullen JR. Molecular distinction between physiological and pathological cardiac hypertrophy: Experimental findings and therapeutic strategies. Pharmacol Ther [Internet]. 2010;128(1):191–227. Available from: http://dx.doi.org/10.1016/j.pharmthera.2010.04.005
- Shioi T, McMullen JR, Kang PM, Douglas PS, Obata T, Franke TF, et al. Akt/protein kinase B promotes organ growth in transgenic mice. Mol Cell Biol. 2002;22(8):2799–809.
- DeBosch B, Treskov I, Lupu TS, Weinheimer C, Kovacs A, Courtois M, et al. Akt1 is required for physiological cardiac growth. Circulation. 2006;113(17):2097–104.
- Boström P, Mann N, Wu J, Quintero P a, Plovie ER, Gupta RK, et al. C/EBPβ controls exercise-induced cardiac growth and protects against pathological cardiac remodeling. Cell. 2010;143(7):1072–83.
- J M, Lu J-R, Antos C, Markham B, Richardson J, Robbins J, et al. A Calcineurin-Dependent Transcriptional Pathway for Cardiac Hypertrophy. Cell. 1998;93(2):215–28.
- Chin ER, Olson EN, Richardson JA, Yang Q, Humphries C, Shelton JM, et al. A calcineurin-dependent transcriptional pathway controls skeletal muscle fiber type. GENES Dev. 1998;12:2499–509.
- Gollnick PD, Armstrong RB, Saltin B, Saubert CW, Sembrowich WL, Shepherd RE. Effect of training composition on enzyme activity and fiber of human ske 1 eta1 muscle. J Appl Physiol. 1973;34(1).
- Rooij E Van, Quiat D, Johnson BA, Sutherland LB, Qi X, Richardson A, et al. A family of microRNAs encoded by myosin genes governs myosin expression and muscle performance. 2009;17(5):662–73.
- Chin ER. Role of Ca2 /calmodulin-dependent kinases in skeletal muscle plasticity. J Appl Physiol. 2005;99:414–23.
- Rose AJ, Kiens B, Richter EA. Ca 2+ -calmodulin-dependent protein kinase expression and signalling in skeletal muscle during exercise. J Physiol [Internet]. 2006;574(3):889–903. Available from: http://doi.wiley.com/10.1113/jphysiol.2006.111757
- Egan B, Zierath JR. Exercise metabolism and the molecular regulation of skeletal muscle adaptation. Cell Metab [Internet]. 2013;17(2):162–84. Available from: http://dx.doi.org/10.1016/j.cmet.2012.12.012
- Gibala MJ, Little JP, Macdonald MJ, Hawley JA. Physiological adaptations to low-volume, high-intensity interval training in health and disease. J Physiol. 2012;590(5):1077–84.
- Wu H, Kanatous S, Thurmond F, Gallardo T, Isotani E, Bassel-Duby R, et al. Regulation of Mitochondrial Biogenesis in Skeletal Muscle by CaMK. Science (80- ). 2002;296:349–52.